Kwasy karboksylowe
| Grupa funkcyjna - grupa karboksylowa −COOH | 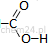 |
Wzór ogólny kwasów karboksylowych R−COOH CnH2n+1COOH (n - ilość atomów węgla w cząsteczce, R- grupa alkilowa lub H-)
Kwasy karboksylowe zbudowane są z grupy alkilowej -R (−CnH2n+1) i grupy karboksylowej −COOH.
Nazwy systematyczne kwasów karboksylowych tworzy się od odpowiednich węglowodorów.
Kwasy karboksylowe tworzą szereg homologiczny, czyli każdy kolejny wzór kwasu posiada o jedną grupę −CH2− więcej od poprzedniego.
| nazwa i wzór węglowodoru | nazwa systematyczna | nazwa zwyczajowa | wzór sumaryczny | wzór półstrukturalny |
| metan CH4 | kwas metanowy | kwas mrówkowy | HCOOH | 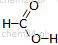 |
| etan C2H6 | kwas etanowy | kwas octowy | CH3COOH | 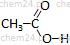 |
| propan C3H8 | kwas propanowy | kwas propionowy | C2H5COOH | 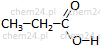 |
| butan C4H10 | kwas butanowy | kwas masłowy | C3H7COOH | 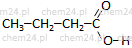 |
Wraz ze zwiększaniem się liczby atomów węgla w cząsteczkach kwasów zmieniają się ich właściwości fizyczne: zmniejsza się ich gęstość, rozpuszczalność w wodzie.
Kwasy, które w cząsteczkach zawierają od 11 atomów węgla nazwywa się wyższymi kwasami tłuszczowymi.
Kwas metanowy
Nazwa zwyczajowa: kwas mrówkowy.
Występowanie: jad mrówek, liście pokrzywy.
Własności fizyczne: bezbarwna ciecz o ostrym zapachu, parząca, trująca, dobrze miesza się z wodą.
Własności chemiczne: ostry zapach, trujący, parzący, bakteriobójczy, ulega reakcji dysocjacji jonwej, reakcji spalania.
W roztworze wodnym kwas metanowy ulega reakcji dysocjacji jonowej:
HCOOH ⇄ H+ + COO–
H+ kation wodoru, COO– anion metanianowy (anion mrówczanowy)
Kwas metanowy ulega reakcji spalania zgodnie z równaniem:
2HCOOH + O2 → 2CO2 + H2O
Kwas etanowy
Nazwa zwyczajowa: kwas octowy
• Właściwości fizyczne
W temperaturze pokojowej kwas etanowy jest bezbarwną cieczą, dobrze miesza się z wodą.
• Właściwości chemiczne
Charakterystyczny zapach, ulega reakcjom spalania, reaguje z aktywnymi metalami, tlenkami metali i zasadami tworząc sole.
Kwas etanowy ulega reakcji spalania całkowitego:
CH3COOH + 2O2 → 2CO2 + 2H2O
Otrzymywanie - fermentacja octowa. Przebiega z udziałem bakterii octowych, które utleniają etanol do kwasu etanowego.
C2H5OH + O2 —bakterie→ CH3COOH + H2O
Reakcja dysocjacji jonowej
CH3COOH —H2O→ H+ + COO−
Kwas etanowy w roztworze wodnym dysocjuje na kationy wodoru H+ i aniony etanianowe (octanowe) COO− .
Odczyn: kwasowy.
Papierek wskaźnikowy zwilżony kwasem przybiera barwę czerwoną.
Oranż metylowy po dodaniu do kwasu zmienia barwę z pomarańczowej na czerwoną.
Reakcje z metalami
2CH3COOH + 2Na → 2CH3COONa + H2
Kwas etanowy reaguje z sodem i powstaje etanian sodu (octan sodu) i wodór.
2CH3COOH + Mg → (CH3COO)2Mg + H2 (etanian magnezu, octan magnezu)
Kwas etanowy reaguje z magnezem i powstaje etanian magnezu (octan magnezu) i wodór.
CH3COONa i (CH3COO)2Mg są to sole kwasu etanowego.
Reakcje z zasadami - reakcje zobojętniania
NaOH + CH3COOH → CH3COONa + H2O
Wodorotlenek sodu reaguje z kwaem etanowym i powstaje etanian sodu i woda.
Etanian sodu CH3COONa jest solą kwasu etanowego.
Zapis jonowy reakcji:
Na+ + OH− + CH3COO− + H+ → CH3COO− + Na+ + H2O
Zapis jonowy skrócony:
H+ + OH− → H2O
Po dodaniu kwasu etanowego do roztworu NaOH z dodatkiem fenoloftaleiny obserwuje się odbarwienie roztworu.
Reakcje z tlenkami metali
ZnO + 2CH3COOH → (CH3COO)2Zn + H2O
Tlenek cynku(II) reaguje z kwasem etanowym i powstaje etanian cynku(II) (octan cynku(II)).
CuO + 2CH3COOH → (CH3COO)2Cu + H2O
Tlenek miedzi(II) reaguje z kwasem etanowym i powstaje etanian miedzi(II) (octan miedzi(II)).
Zastosowanie kwasu etanowego:
- konserwowanie produktów spożywczych (ocet to10% kwas etanowy)
Zapraszam do wpisania komentarza: uwagi, co jeszcze dopisać, objaśnić, sprecyzować, niezrozumiała treść, błędy itp.
Napisz komentarz
Treść strony i wszystkie elementy strony chem24.pl podlegają ochronie prawnej zawartej w przepisach o prawie autorskim.
Niedozwolone jest kopiowanie, rozpowszechnianie i udostępnianie innym użytkownikom bez zgody autora.
Niedozwolone działania stanowią okradanie autora i podlegają przepisom zawartym w Kodeksie Karnym.
