Węglowodory nienasycone
Węglowodory nienasycone - mają w cząsteczce wiązania podwójne C=C lub potrójne C≡C.
Alkeny
W cząsteczkach alkenów znajduje się wiązanie podwójne. Nazwę alkenu rozpoznaje się po końcówce −en.
Wzór ogólny szeregu homologicznego alkenów CnH2n
| eten (etylen) | C2H4 | CH2=CH2 | 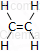 |
| propen | C3H6 | CH2=CH−CH3 | 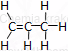 |
| buten | C4H8 | CH2=CH−CH2−CH3 | 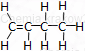 |
Reakcje spalania
C2H4 + 3O2 → 2CO2 + 2H2O spalanie całkowite
C2H4 + 2O2 → 2CO + 2H2O spalanie niecałkowite (półspalanie)
C2H4 + O2 → 2C + 2H2O spalanie niecałkowite
Przyłączenie wodoru (addycja)
CH2=CH2 + H2 → CH3−CH3
eten etan

Przyłączanie bromu (addycja)
CH2=CH2 + Br2 → CH2Br−CH2Br
eten + brom → 1,2-dibromoetan
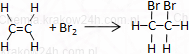
Przyłączanie chlorowodoru (addycja)
CH2=CH2 + HCl → CH3−CH2Cl
eten + chlorowodór → chloroetan
Polimeryzacja - reakcja łączenia dużej ilości cząsteczek związków nienasyconych (merów) i tworzenie związku wielkocząsteczkowego (polimeru)
Polimeryzacja etenu
n CH2=CH2 → -[−CH2−CH2−]−n
eten polieten (polietylen)

Zastosowanie etenu
- w przemyśle chemicznym przy produkcji polietylenu i innych związków chemicznych
- w ogrodnictwie - przyspiesza dojrzewanie owoców
Zastosowanie polietylenu (PE)
Polietylen (PE) to tworzywo sztuczne o szerokim zastosowaniu ze względu na jego właściwości: jest lekkie, ma dużą odporność na uderzenia, nie wchłania wilgoci, odporne na działanie wielu czynników chemicznych, nie przewodzi prądu elektrycznego.
Robi się z niego folie spożywcze, naczynia jednorazowe, nakrętki, torby zakupowe, zabawki, butelki, folie termokurczliwe i wiele innych elementów.
Alkiny
Wzór ogólny CnH2n-2, W nazwie posiadają końcówkę -in lub -yn.
| etyn (acetylen) | HC≡CH | H−C≡C−H |
| propyn | HC≡C−CH3 | 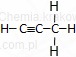 |
Reakcje spalania
2C2H2 + 5O2 → 4CO2 + 2H2O
2C2H2 + 3O2 → 4CO + 2H2O
2C2H2 + O2 → 4C + 2H2O
Reakcja etynu z wodorem
HC≡CH + H2 → CH2=CH2 (eten)
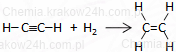
HC≡CH + 2H2 → CH3−CH3 (etan)
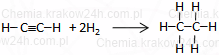
Reakcja etynu z bromem (lub chlorem)
HC≡CH + Br2 → CHBr=CHBr (1,2-dibromoeten)
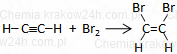
HC≡CH + 2Br2 → CHBr2−CHBr2 (1,1,2,2-tetrabromoetan)

Reakcja etynu z chlorowodorem (lub bromowodorem)
HC≡CH + HCl → CH2=CHCl (chloroeten)

Zapraszam do wpisania komentarza: uwagi, co jeszcze dopisać, objaśnić, sprecyzować, niezrozumiała treść, błędy itp.
Napisz komentarz
Treść strony i wszystkie elementy strony chem24.pl podlegają ochronie prawnej zawartej w przepisach o prawie autorskim.
Niedozwolone jest kopiowanie, rozpowszechnianie i udostępnianie innym użytkownikom bez zgody autora.
Niedozwolone działania stanowią okradanie autora i podlegają przepisom zawartym w Kodeksie Karnym.
