Aminy
Aminy to pochodne amoniaku (NH3), gdzie atomy wodoru są zastąpione grupami węglowodorowymi.
(R) Rzędowość amin ⇒ odpowiada ilości atomów wodoru, które zostały zastąpione przez grupy -R (mogą być różne).
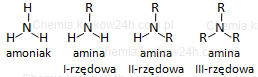
−NH2 - grupa aminowa (grupa funkcyjna)
-R - grupa węglowodorowa alifatyczna (może być również aromatyczna -Ar)
Wzór ogólny amin I-rzędowych: R-NH2 , Ar-NH2
| Atom azotu w aminach ma hybrydyzację sp3.Orbitale tworzą 3 wiązania σ N−H a na czwartym znajduje się wolna para elektronowa azotu. | 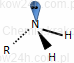 |
Nazewnictwo (*nazwa preferowana IUPAC)
Dwa możliwe sposoby nazewnictwa pierwszorzędowych amin:
(1) Do słowa −amina dodaje się w przedrostku nazwę węglowodoru.
(2) Do słowa −amina dodaje się w przedrostku nazwę grupy alkilowej lub arylowej przyłączonej do atomu azotu (tylko dla monoamin).
Anilina jest nazwą preferowaną przez IUPAC.
| CH3−NH2 | CH3−CH2−NH2 | 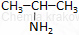 |
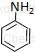 |
| (1) metanoamina* (2) metyloamina |
(1) etanoamina* |
(1) propano-2-amina* | anilina* (1) benzenoamina (2) fenyloamina, |
Masz już w sobie przekonanie, że potrzebujesz wsparcia, aby odkryć fascynujący świat chemii, w codziennej nauce i przygotowaniu do matury?
Załóż konto
Zyskaj dostęp do artykułów, które przekształcą skomplikowane zagadnienia chemiczne w zrozumiałe i interesujące treści.
Każdy artykuł, który przeczytasz, zwiększy Twoje zrozumienie i zaciekawienie chemią.
Nie czekaj, zacznij swoją naukową podróż już dziś!
Załóż konto
Zyskaj dostęp do artykułów, które przekształcą skomplikowane zagadnienia chemiczne w zrozumiałe i interesujące treści.
Każdy artykuł, który przeczytasz, zwiększy Twoje zrozumienie i zaciekawienie chemią.
Nie czekaj, zacznij swoją naukową podróż już dziś!
| Pełny tekst dostępny jest tylko dla zalogowanych |
Copyright 2011-2024Chem24.pl
Wszelkie prawa autorskie do treści zawartych w serwisie chem24.pl należą do właściciela portalu.
Treść strony i wszystkie elementy strony chem24.pl podlegają ochronie prawnej zawartej w przepisach o prawie autorskim.
Niedozwolone jest kopiowanie, rozpowszechnianie i udostępnianie innym użytkownikom bez zgody autora.
Niedozwolone działania stanowią okradanie autora i podlegają przepisom zawartym w Kodeksie Karnym.
Treść strony i wszystkie elementy strony chem24.pl podlegają ochronie prawnej zawartej w przepisach o prawie autorskim.
Niedozwolone jest kopiowanie, rozpowszechnianie i udostępnianie innym użytkownikom bez zgody autora.
Niedozwolone działania stanowią okradanie autora i podlegają przepisom zawartym w Kodeksie Karnym.
