Alkohole monohydroksylowe
Budowa cząsteczek alkoholi
Alkohole - pochodne węglowodorów, które w cząsteczkach mają grupę -OH zamiast jednego lub kilku atomów wodoru
Grupa funkcyjna alkoholi: -OH, grupa hydroksylowa
Grupa alkilowa - część cząsteczki alkanu bez jednego atomu wodoru.
Np. −CH3, −C2H5 ogólnie oznaczana jako -R.
Alkohole monohydroksylowe zbudowane są z grupy alkilowej -R i jednej grupy hydroksylowej -OH.
Alhohole polihydroksylowe mają więcej niż jedną grupę hydroksylową -OH.
Wzór ogólny alkoholi monohydroksylowych: CnH2n+1OH lub R-OH
Wzory i nazwy wybranych alkoholi monohydroksylowych
Tworzenie nazw alkoholi: nazwę tworzy się od nazwy węglowodoru dodając końcówkę -ol
Tworzenie wzorów: w cząsteczce alkanu zamiast jednego atomu wodoru pisze się grupę -OH
| węglowodór | alkohol | wzór grupowy | wzór półstrukturalny | wzór strukturalny |
| metan | metanol alkohol metylowy |
CH3OH | CH3–OH | 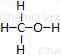 |
| etan | etanol alkohol etylowy |
C2H5OH | CH3–CH2–OH | 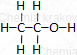 |
| propan | propanol alkohol propylowy |
C3H7OH | CH3–CH2–CH2–OH | 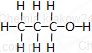 |
| butan | butanol alkohol butylowy |
C4H9OH | CH3–CH2–CH2–CH2–OH | 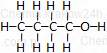 |
Własności metanolu i etanolu
| metanol (CH3OH) | etanol (C2H5OH) |
| Bezbarwna, lotna ciecz | Bezbarwna, lotna ciecz |
| Charakterystyczny, ostry zapach | Charakterystyczny, przyjemny zapach |
| Dobrze miesza się z wodą | Dobrze miesza się z wodą |
| Gęstość mniejsza od wody (0,79 g/cm³) | Gęstość mniejsza od wody (0,79 g/cm³) |
| Temperatura wrzenia: 64,7°C. | Temperatura wrzenia: 78,4°C. |
| Jest łatwopalny, spalając się w płomieniu o niebieskiej barwie. Silnie toksyczny – spożycie nawet niewielkich ilości może prowadzić do ślepoty lub śmierci. |
Łatwopalny, spalając się w płomieniu o niebieskiej barwie. |
Spalanie metanolu i etanolu
Spalanie całkowite
2CH3OH + 3O2 → 2CO2 + 4H2O
C2H5OH + 3O2 → 2CO2 + 3H2O
Spalanie niecałkowite
CH3OH + O2 → CO + 2H2O
C2H5OH + 2O2 → 2CO + 3H2O
lub
2CH3OH + O2 → 2C + 4H2O
C2H5OH + O2 → 2C + 3H2O
Negatywny wpływ metanolu i etanolu na organizm człowieka
Metanol (CH₃OH):
-
Toksyczność:
- Metanol jest silnie toksyczny, nawet w niewielkich ilościach. Spożycie już około 10 ml może powodować poważne zatrucia, w tym trwałą ślepotę, a dawka 30–50 ml może być śmiertelna.
- Po spożyciu metanol jest metabolizowany w wątrobie do formaldehydu (CH₂O) i kwasu mrówkowego (HCOOH), które są toksyczne dla organizmu.
-
Wpływ na organizm:
- Ośrodkowy układ nerwowy: Zatrucie metanolem może powodować ból głowy, zawroty, osłabienie, senność, a w ciężkich przypadkach śpiączkę.
- Układ wzrokowy: Kwas mrówkowy gromadzi się w nerwie wzrokowym, co prowadzi do uszkodzenia siatkówki i ślepoty.
- Metaboliczna kwasica: Nadmiar kwasu mrówkowego zakwasza krew, co może prowadzić do uszkodzenia narządów i śmierci.
-
Objawy zatrucia:
- Ból głowy, zawroty głowy, osłabienie.
- Nudności, wymioty.
- Zaburzenia widzenia, które mogą prowadzić do całkowitej ślepoty.
- Zaburzenia oddechowe i śpiączka.
Etanol (C₂H₅OH):
-
Toksyczność:
- Etanol jest mniej toksyczny niż metanol, ale jego nadmierne spożycie może powodować ostre i przewlekłe zatrucia.
- W organizmie utlenia się do aldehydu octowego (CH₃CHO) i kwasu octowego (CH₃COOH), które w nadmiarze są szkodliwe.
-
Wpływ na organizm:
- Ośrodkowy układ nerwowy: Etanol działa depresyjnie, powodując osłabienie funkcji mózgu, utratę kontroli nad ruchem i mową. W dużych dawkach prowadzi do śpiączki i śmierci.
- Układ pokarmowy: Podrażnia błonę śluzową żołądka, co może powodować zapalenie i wrzody.
- Wątroba: Przewlekłe spożywanie prowadzi do stłuszczenia wątroby, zapalenia, a w końcu do marskości.
- Układ krążenia: Nadmiar etanolu zwiększa ryzyko nadciśnienia i chorób serca.
-
Objawy zatrucia:
- Euforia, zaburzenia koordynacji ruchowej.
- Nudności, wymioty.
- Obniżenie świadomości, śpiączka.
- Zatrzymanie oddechu i śmierć w przypadku ostrego zatrucia.
Porównanie wpływu metanolu i etanolu:
- Metanol: Skrajnie toksyczny, powoduje ciężkie zatrucia nawet w małych dawkach. Jego głównym zagrożeniem jest ślepota i szybka śmierć.
- Etanol: Stosowany w kontrolowanych ilościach jako składnik napojów alkoholowych, ale nadużywany prowadzi do uzależnienia, uszkodzenia narządów i problemów zdrowotnych.
Metanol i etanol, mimo ich szerokiego zastosowania, wymagają ostrożnego użytkowania. Spożycie metanolu jest zawsze niebezpieczne, natomiast nadmierne spożycie etanolu niesie poważne konsekwencje zdrowotne. Edukacja i odpowiedzialność są kluczowe w minimalizowaniu ryzyka związanego z tymi substancjami.
Zastosowania metanolu i etanolu
Metanol (CH₃OH):
Metanol, znany również jako alkohol metylowy, ma szerokie zastosowania w przemyśle chemicznym i energetycznym, ale jest toksyczny dla organizmów żywych.
-
Przemysł chemiczny:
- Produkcja formaldehydu: Podstawowy surowiec do syntezy formaldehydu, który jest używany w produkcji żywic, tworzyw sztucznych i farb.
- Synteza innych chemikaliów: Stosowany do produkcji metanolanów, estrów oraz kwasu octowego.
-
Przemysł paliwowy:
- Biopaliwa: Dodatek do paliw, np. biodiesla, lub jako paliwo w silnikach spalinowych.
- Ogniwa paliwowe: Wykorzystywany jako źródło energii w nowoczesnych ogniwach paliwowych.
-
Rozpuszczalnik:
- Używany w procesach chemicznych i laboratoriach jako rozpuszczalnik organiczny.
-
Chłodziwa i płyny przemysłowe:
- Wykorzystywany w płynach do odmrażania szyb i chłodnic.
-
Środek denaturujący:
- Dodawany do etanolu, aby uczynić go niezdatnym do spożycia.
Etanol (C₂H₅OH):
Etanol, znany również jako alkohol etylowy, jest jednym z najbardziej wszechstronnych związków organicznych. Jest bezpieczniejszy od metanolu, ale nadal wymaga ostrożnego stosowania.
-
Przemysł spożywczy:
- Napoje alkoholowe: Główny składnik alkoholu w winach, piwach i mocniejszych trunkach.
- Konserwant: Wykorzystywany w ograniczonym stopniu w żywności.
-
Przemysł farmaceutyczny:
- Środek dezynfekcyjny: Stosowany w roztworach odkażających do skóry i powierzchni.
- Rozpuszczalnik: Używany w produkcji syropów, leków i ekstraktów roślinnych.
-
Przemysł kosmetyczny:
- Składnik perfum, dezodorantów i płynów kosmetycznych.
-
Przemysł energetyczny:
- Biopaliwo: Składnik paliw samochodowych (np. E10, E85) lub samodzielne paliwo w specjalnych silnikach.
-
Przemysł chemiczny:
- Surowiec do produkcji związków takich jak eter dietylowy czy octan etylu.
-
Środek czyszczący:
- Używany w produktach do mycia szyb, elektroniki i powierzchni.
Podsumowanie:
- Metanol znajduje zastosowanie głównie w przemyśle technicznym i energetycznym, ale jego toksyczność ogranicza możliwość bezpośredniego kontaktu z człowiekiem.
- Etanol jest bardziej wszechstronny i stosowany zarówno w przemyśle spożywczym, farmaceutycznym, kosmetycznym, jak i energetycznym. Jego właściwości czynią go niezbędnym w życiu codziennym i gospodarce.
Kontrakcja objętości
Kontrakcja objętości to zjawisko fizyczne, polegające na zmniejszeniu łącznej objętości mieszaniny dwóch cieczy po ich zmieszaniu, w porównaniu do sumy objętości tych cieczy przed zmieszaniem.
Przykład kontrakcji objętości:
- Zmieszanie wody i alkoholu etylowego:
Jeśli zmieszamy np. 50 ml wody z 50 ml etanolu, otrzymana mieszanina nie będzie miała 100 ml, ale mniej (np. ok. 96-97 ml).
Przyczyna kontrakcji objętości:
Zjawisko to wynika z różnic w budowie cząsteczek i interakcji między nimi:
- Cząsteczki jednej cieczy wnikają w wolne przestrzenie między cząsteczkami drugiej cieczy.
- W przypadku wody i alkoholu etylowego, mniejsze cząsteczki wody mogą zajmować puste przestrzenie pomiędzy większymi cząsteczkami etanolu, co prowadzi do zmniejszenia łącznej objętości.
Znaczenie praktyczne kontrakcji objętości:
-
Przemysł spożywczy i chemiczny: Uwzględnia się kontrakcję objętości w procesach mieszania substancji, aby precyzyjnie określić ilości mieszanin.
-
Produkcja roztworów: W chemii kontrakcja objętości jest brana pod uwagę podczas przygotowywania roztworów o dokładnych stężeniach.
Fermentacja alkoholowa
Fermentacja alkoholowa to proces biochemiczny, w którym cukry (np. glukoza, fruktoza) są przekształcane przez drożdże lub inne mikroorganizmy w alkohol etylowy (etanol) i dwutlenek węgla (CO₂) w warunkach beztlenowych.
Równanie reakcji fermentacji alkoholowej
Proces ten można zapisać w postaci równania chemicznego:
C6H12O6 —enzymy→ 2 C2H5OH + 2 CO2 + energia
Glukoza —enzymy→ etanol + dwutlenek węgla
Warunki fermentacji alkoholowej
-
Beztlenowe środowisko: Proces zachodzi przy braku tlenu, ponieważ w obecności tlenu mikroorganizmy przekształcają cukry w wodę i CO₂, a nie w alkohol.
-
Obecność drożdży: Drożdże, np. z rodzaju Saccharomyces cerevisiae, zawierają enzymy (m.in. zymazę), które katalizują reakcje fermentacji.
-
Temperatura: Optymalna temperatura to 20–30°C. Zbyt wysoka temperatura (powyżej 40°C) może zabić drożdże.
-
Obecność cukrów: Cukry proste, takie jak glukoza lub fruktoza, są najłatwiej fermentowane.
Znaczenie fermentacji alkoholowej
-
Przemysł spożywczy: Produkcja alkoholi: piwa, wina, spirytusu. Produkcja pieczywa – powstały podczas fermentacji CO₂ powoduje wyrastanie ciasta.
-
Przemysł chemiczny: Produkcja etanolu wykorzystywanego jako rozpuszczalnik, surowiec chemiczny czy dodatek do paliw (bioetanol).
-
Biotechnologia: Fermentacja jest wykorzystywana w bioprodukcji różnych związków chemicznych i leków.
Przykłady w życiu codziennym
- Fermentacja w winogronach podczas produkcji wina.
- Proces wytwarzania piwa w browarach.
- Wzrost ciasta drożdżowego dzięki CO₂ uwalnianemu podczas fermentacji.
Fermentacja alkoholowa to kluczowy proces w przemyśle spożywczym i biotechnologicznym, który od tysięcy lat wspiera rozwój cywilizacji.
